Carolyn Bertozzi, la Premio Nobel que cambió el matraz por la célula.
El grupo de Bertozzi denominó química bioortogonal al conjunto de reacciones químicas que pueden realizarse en el interior de una célula sin que afecten a sus biomoléculas ni a los procesos bioquímicos que ocurren en ella. Imagino que la denominación deriva de la ortogonalidad matemática (perpendicularidad) que en química interpretaríamos como reacciones independientes que no se ven afectadas unas por las otras.
https://pubs.acs.org/doi/10.1021/acs.bioconjchem.1c00461
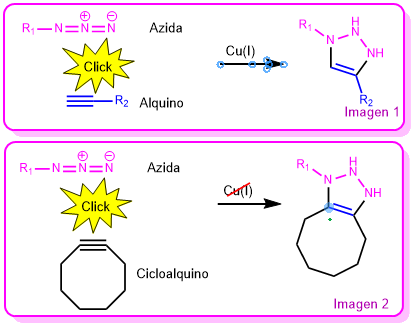
Bertozzi encontró en la «química del click» de Sharpless una reacción que podía ser llevada a cabo en medio acuoso, a temperatura ambiente y pH fisiológico. Además, esta reacción tiene unos componentes que son ajenos a la vida (azida y alquino) y por tanto no interfieren con los procesos bioquímicos de la célula, salvo por el detalle de ser catalizada por cobre (I), una sustancia que presenta citotoxicidad. En ausencia de cobre la reacción precisa temperaturas de unos 100ºC, también incompatibles con la célula.(Imagen 1)
Para evitar el uso del cobre(I) Bertozzi utiliza su magia y cambia el alquino lineal por uno cíclico, la tensión que posee ese anillo impulsa la reacción hacia el producto sin necesidad de emplear el catalizador de Cu(I). Ahora ya puede realizar la reacción entre el alquino y la azida en condiciones totalmente compatibles con la vida. La elección del ciclooctino no es casual, se trata del alquino cíclico de menor tamaño con estabilidad. (Imagen 2)
Lo sé, lo sé, estarás pensando, ¿y para qué va interesar formar un triazol en el interior de una célula?. Pues es la forma más genial de marcar mediante una sonda fluorescente proteínas, lípidos, glúcidos y ácidos nucleicos para estudiar diferentes procesos celulares.
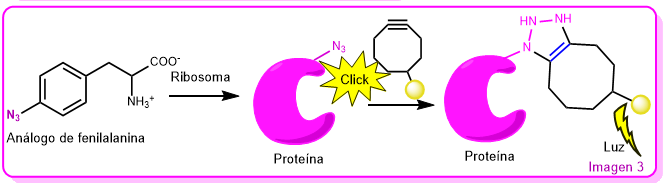
Veamos el etiquetado de una proteína. Al aportar a la célula un aminoácido modificado con un grupo azida, por ejemplo la 4-azido-1-fenilalanina, el ribosoma lo confunde con la fenilalanina y lo incorpora a la proteína. A continuación, se suminitra el alquino con la sonda fluorescente y se produce la reacción de «click» que une los grupos azida con el alquino. El resultado es la formación de una proteína fluorescente. (Imagen 3)
https://pubs.acs.org/doi/10.1021/acs.jproteome.5b00653
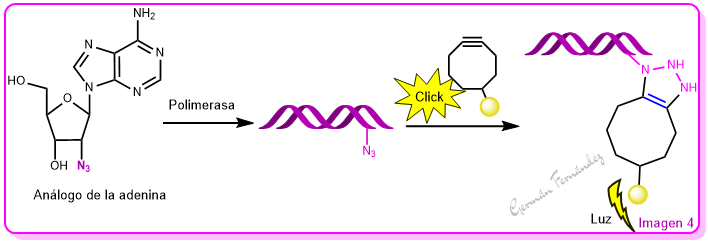
Etiquetado de ácidos nucleicos. El aporte de nucleótidos análogos, que poseen grupos azida, hace que las polimeraras los incorporen a las moléculas de ADN o ARN. La reacción posterior con un ciclooctino con sonda fluorescente permite hacer visibles estos nucleótidos. (imagen 4).
https://onlinelibrary.wiley.com/…/10.1002/tcr.202100322

